香港科技大學(科大)研究人員發明了一種名為「CarGAP」的突破性微觀通道調控工具,可利用維生素B₁₂和綠光精確控制間隙連接,使細胞之間得以直接而可控地進行通訊。透過精確、按需要地關開細胞間的橋樑,這項新技術為調控細胞間關鍵分子和電訊號的流動提供了前所未有的時空精度。該工具已在哺乳類動物細胞和活體果蠅中得到驗證,為研究發育、免疫及神經活動提供了有效的新途徑,並對理解疾病機制和推進再生醫學研究具有深遠潛力。
間隙連接對維持生命基本功能至關重要。這些通道負責細胞間離子、第二信使和小分子的直接傳遞,從而協調包括心跳與大腦功能在內的多種細胞活動。當間隙連接功能失調時,可能引發心血管疾病、發育異常,甚至癌症。然而,研究其精確功能一直頗具挑戰。傳統的基因敲除方法具有不可逆轉且不夠精確的限制,而化學抑製劑則往往缺乏特異性,並可能產生毒性。因此,開發一種能夠如開關般進行精細、低副作用地調控間隙連接技術,已成為細胞生物學和神經生物學領域長期的關鍵需求。
研究的核心挑戰在於建立一種既可逆轉且具生物兼容性、又不干擾細胞自然過程的間隙連接調控策略。現有的光遺傳學工具多依賴具有潛在光毒性的藍光,而化學方法則普遍缺乏空間精確度。基於上述限制,研究團隊因此致力開發一套可基因編碼、能響應無害刺激、並可廣泛應用於從人類細胞到複雜模式生物(如果蠅)的通用調控系統。
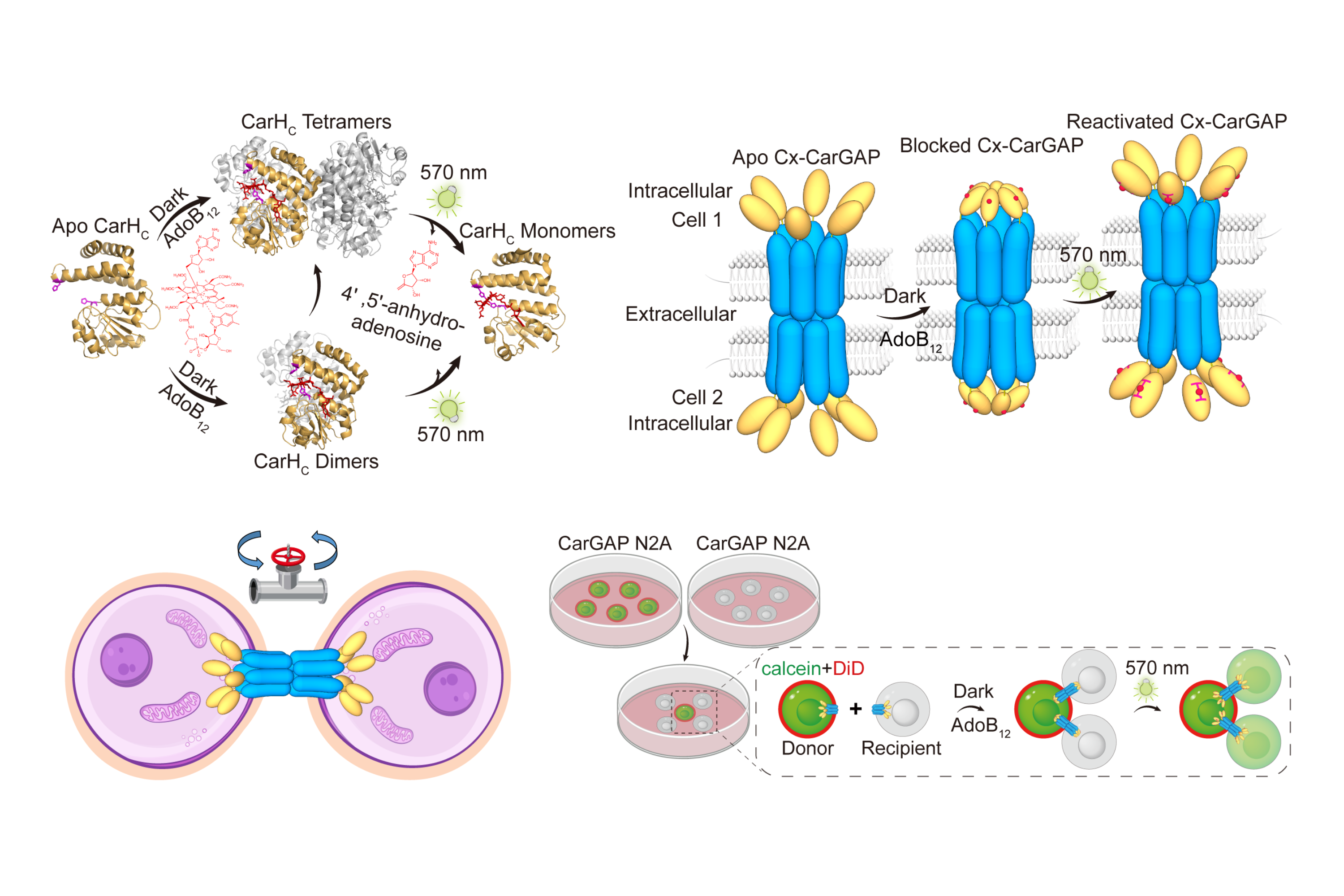
由科大化學及生物工程學系教授孫飛教授、嘉里理學教授兼生命科學部講座教授解亭教授、生命科學部前研究助理教授屠仁軍教授(現為南京東南大學教授),以及北京大學化學與分子工程學院鄒鵬教授合作領導的團隊,通過將間隙連接蛋白(脊椎動物的連接蛋白connexins和無脊椎動物的innexins)與一種來自細菌CarHC蛋白的光敏維生素B₁₂結合域融合,成功開發出CarGAP系統。在黑暗條件下,添加維生素B₁₂(AdoB12)會誘導CarHC結構域發生寡聚,從而物理性堵塞通道;而施加柔和的綠光(570 nm)則可促使這些蛋白阻塞物解聚,重新開放通道。這一精巧設計使研究人員能通過簡單的維生素實現通道關閉,再通過光照實現通道重新開啟。
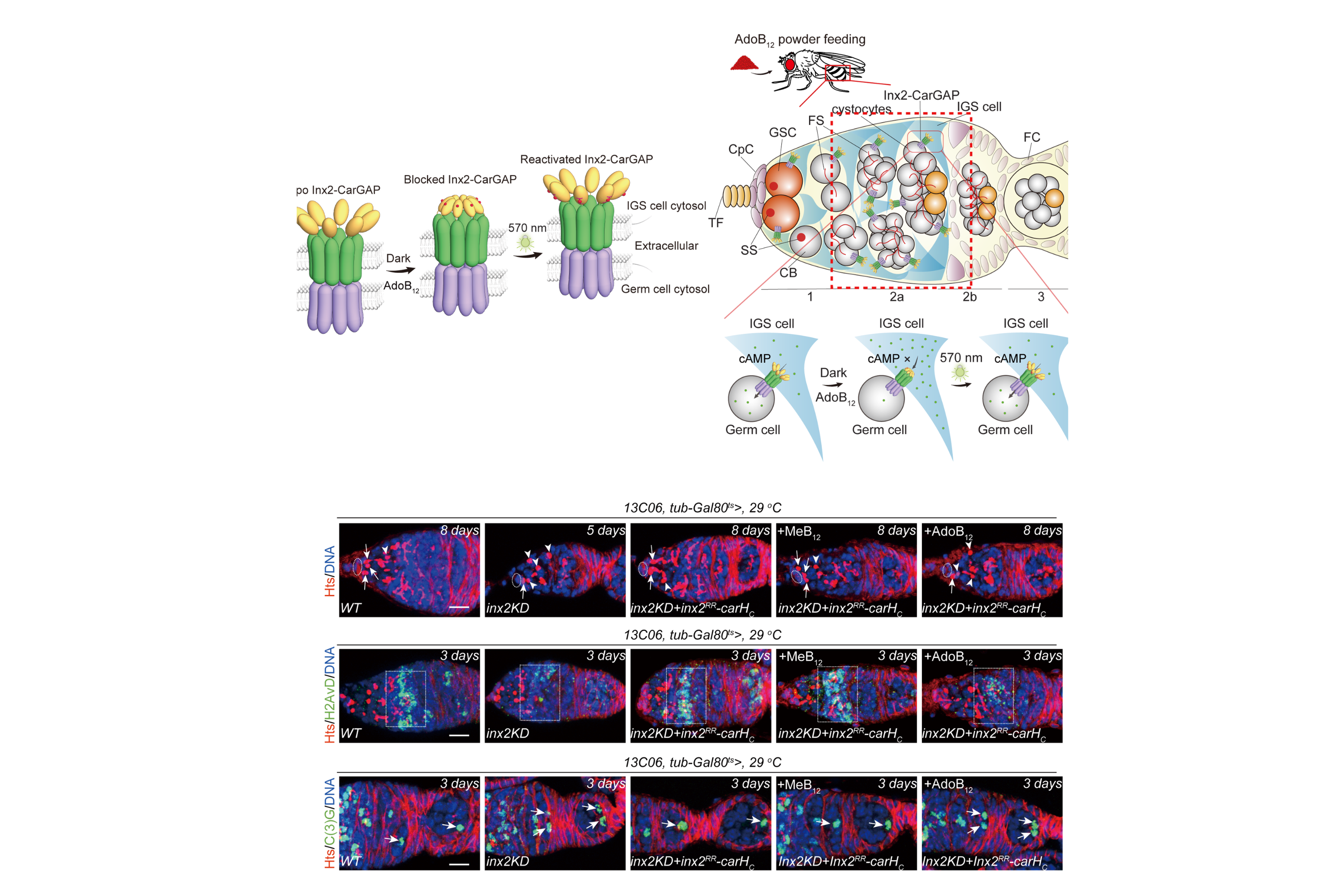
研究團隊在多個層面上驗證了CarGAP的功能:他們成功調控了熒光染料及免疫信號分子2’3’-cGAMP在哺乳類動物細胞間的傳遞,並利用遠紅電壓傳感器NAVI-Cy5,光學記錄了光照後細胞間電耦合的恢復。最令人矚目的是,團隊將CarGAP引入活體果蠅卵巢,成功阻斷了幹細胞與支持性微環境細胞之間關鍵信號分子cAMP的流動,並在光照後恢復其流動,從而直接影響了幹細胞行為及卵子發育過程。
孫飛教授表示:「CarGAP為我們提供了一種能夠遠程操控細胞最基礎通訊模式的工具。透過結合維生素B₁₂的生物兼容性與光調控的精準性,我們現在可以實時探究細胞如何協調行為——無論是在胚胎、大腦還是腫瘤中。這項工具為理解細胞的動態語言打開了一扇新的窗口。」
這項研究成果已於《美國國家科學院院刊》上發表,論文題為「維生素B₁₂與光協同調控的間隙連接」。研究的共同第一作者包括孫教授的博士生崔舵、黄鑫彧,以及北京大學博士後研究員劉書彰博士。